Tech Sheet on Tofacitinib Citrate
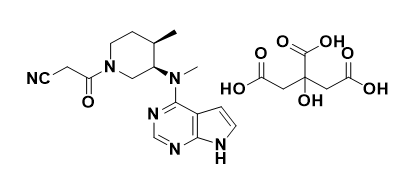
Tofacitinib Citrate (Xeljanz) is an oral, small molecule drug used to treat adults with moderate to severe active rheumatoid arthritis (RA), active psoriatic arthritis, and moderate to severe ulcerative colitis. Tofacitinib works by blocking the body’s production of enzymes called Janus kinases (JAKs). Tofacitinib citrate is the first oral JAK inhibitor approved for use in chronic ulcerative colitis
The global drug sales of Tofacitinib (Xeljanz®) stood at 2.6 billion USD in 2022 and recorded a historical growth (CAGR) of 22% between 2017 to 2022. In addition, before losing patent protection in 2026, it is expected that Tofacitinib will witness peak sales at $2.8 billion in 2025.
Dr. Reddy's API Offering
- Crystalline polymorphic form
- Customized particle size distribution (PSD), which plays a vital role in the formulation development.
- Our process involves efficient chemical transformations that offer a distinctive advantage concerning quality and manufacturability.
We manufacture Tofacitinib citrate API at our cGMP API manufacturing facility, successfully inspected by international regulatory authorities - USFDA, KFDA, WHO-GMP, Russian federation, and ANVISA (document-based inspection completed and certificate is available).
To know more about our API offerings, please read the Tech sheet on Tofacitinib citrate API by filling the contact form below.
Explore other Whitepapers:
Know More- Email us: api@drreddys.com
-
 +91 40 49002222
+91 40 49002222
Download Now
Complete el formulario de contacto a continuación para ver el documento técnico


